铁死亡是近几年备受关注的医学热点话题,我们知道铁死亡在肿瘤细胞中的作用已被广泛验证,但铁死亡与T细胞生物学的研究非常有限。最近,一篇发表于Immunity(IF:43.474)的关于抑制芳基烃受体(Ahr)可防止氧化应激和肠上皮内淋巴细胞铁死亡的文章,重点描述了Ahr抑制因子(Ahrr)维持肠上皮内淋巴细胞 (IEL) 的重要性,提出必须严格调控Ahr 信号以防止氧化应激和IEL的铁死亡并保持肠道免疫反应。那么Ahrr抑制氧化应激以及肠上皮淋巴细胞铁死亡的机制到底是什么呢?

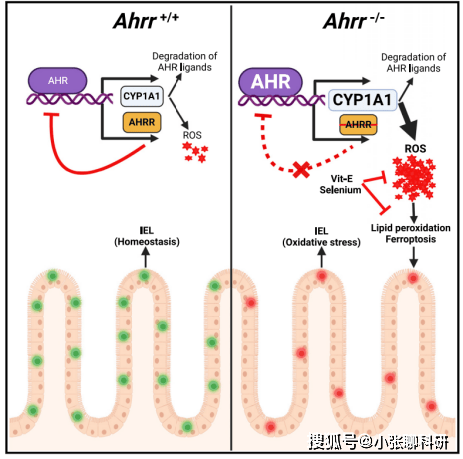
我们知道,Ahr是一种配体激活的转录因子,可促进肠道免疫反应。在胃肠系统中,Ahr通路与免疫系统、肠神经系统共同维持上皮细胞的健康。Ahr对IEL的发育、稳定以及维持屏障功能的作用都是必需的,Ahr也是肠固有层(LP)中免疫细胞的发育和功能所必需的。IEL不断感知波动的环境成分,如共生细菌、致病菌、病原体和饮食成分,有助于维持肠道上皮细胞的稳态及完整性。此外,IEL介导针对各种病原体的免疫反应,在食物不耐受和慢性炎症性肠病 (IBD) 模型中具有保护作用。
既然Ahr是维持肠道免疫所必需,IEL依赖Ahr进行维护并表达 Ahrr负向调节Ahr,作者假设Ahrr缺乏可能会增加肠道中IEL的存在,结果却截然相反,那么出现这种情况的原因是什么呢,接下来让我们来看一下作者是怎样进行研究的吧。
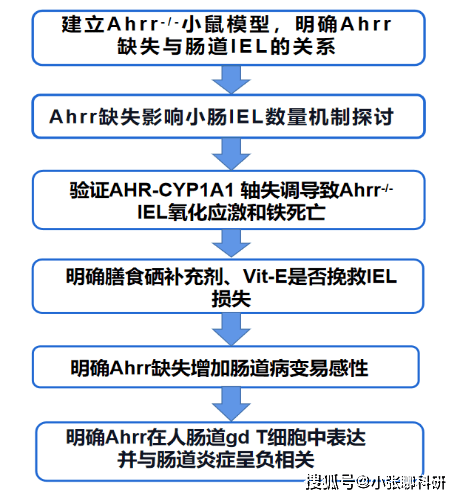
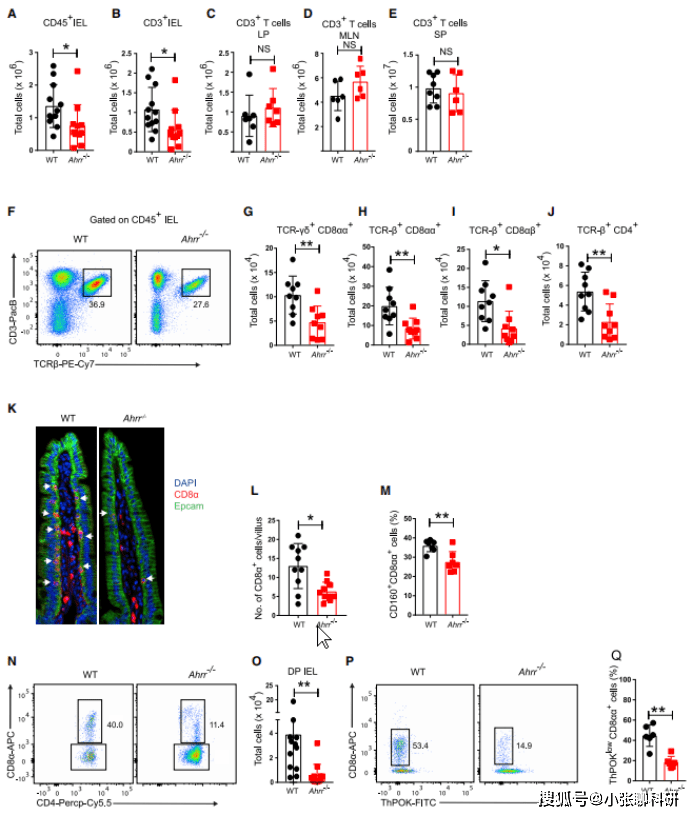
为了确定Ahrr缺乏与IEL之间存在怎样的关系,作者通过免疫荧光、流式细胞术等技术检测出Ahrr-/-小鼠的大小肠上皮内T细胞、IEL的各种子集相较于WT小鼠组显著减少。在对回肠组织中CD8α的染色证实了Ahrr-/-小鼠中IEL的减少,提示Ahrr缺失与IEL数量显著减少相关,但Ahrr缺失不会影响每个细胞IEL的生成水平。那么Ahrr基因剂量是否会影响IEL水平呢?作者比较了WT小鼠和单倍体不足的Ahrr+/-小鼠IEL子集,发现Ahrr基因剂量对IEL存在部分影响。
作者进一步检测了Ahrr缺乏对表达Ahrr并依赖Ahr发育的LP淋巴细胞的影响,发现Ahrr在IELs中的表达明显高于LP T细胞,这可能是IELs更容易出现Ahrr缺失的部分原因(图1)。
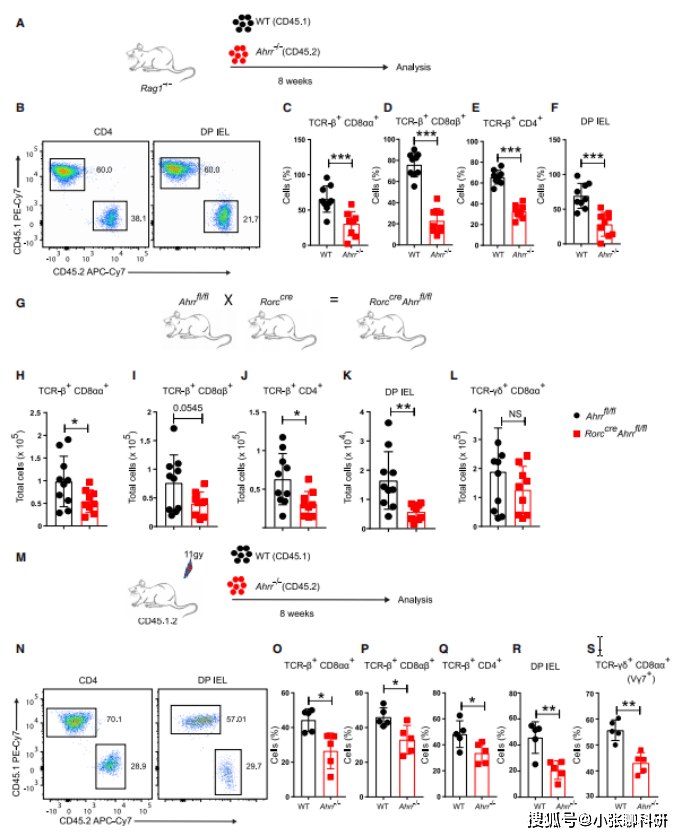
现在我们知道了Ahrr在维护IEL,那么Ahrr对IEL的维持是细胞内在的还是细胞外在的呢?作者对Rag1-/-小鼠进行WT(CD45.1)和Ahrr-/-(CD45.2)小鼠脾脏T细胞的过继转移,8周后检测不同受体小鼠IEL子集水平,发现WT重组小鼠TCRαβ+CD8αα+、TCRαβ+CD8ab+、TCRαβ+CD4 和 DP IEL的频率和数量明显高于Ahrr-/-重组小鼠,这表明Ahrr对IEL的分化或维持是细胞固有的。但此实验中无法从过继转移的Rag1-/-小鼠的肠道中恢复大量的 gd T 细胞,因此无法确定 Ahrr-/-中gd T细胞的缺陷是否也为细胞固有。
为了验证Ahrr在TCRαβ+IEL 中的细胞固有功能,作者将Ahrrfl/fl小鼠与Rorccre小鼠杂交,使所有T细胞和ILC3中的Ahrr基因被删除,发现杂交小鼠IEL子集的表达显著降低,证实Ahrr在TCRαβ+ IEL发育或维持中的细胞内在功能。此外,作者采用竞争性BM嵌合体实验,用WT(CD45.1)和Ahrr-/-(CD45.2)小鼠的BM细胞重组CD45.1.2小鼠,WT(CD45.1)和Ahrr+/+(CD45.2)小鼠作对照,经过IEL重建检测发现Ahrr-/-组小鼠IEL子集的表达显著低于WT组小鼠,进一步证实了Ahrr的细胞固有功能(图 2)。
我们知道了Ahrr缺失对IEL数量的影响,一个新的问题出现了,Ahrr缺失是如何影响IEL数量的呢?因为TCRαβ+天然IEL是从CD4-CD8-NK1.1-TCRαβ+CD5+胸腺IEL祖细胞 (IELps) 迁移到肠道并在到达富含IL-15的肠道环境后获得CD8αα表达。为此作者观察了WT小鼠和 Ahrr-/-小鼠表达CD4和CD8胸腺细胞群分布和胸腺IELp的频率,发现两组小鼠数据无显著差异,表明Ahrr缺失不影响胸腺IEL的发育。作者同样检测了肠道IEL分化需要的IL-15通过的CD122信号通路,以及促进肠道归巢和组织保留的分子,发现WT小鼠和 Ahrr-/-小鼠中各指标的表达相当。进一步说明了IEL的发育和归巢独立于Ahrr。
为了进一步研究 Ahrr 缺陷影响小肠 IEL 数量的机制,作者对WT和Ahrr-/-小鼠的IEL分类,并通过基于液滴的30scRNA-seq (10X Genomics) 对其进行分析,确定了14个IEL聚类,基因集富集 (GSE) 分析证实,第2簇因记忆/干细胞特征而富集,相对于其他IEL群体,该群体中Ahr 特征丰富,突出了Ahr信号在该细胞亚群的潜在作用。
我们知道ROS的产生代表细胞应激,而Hspa1a和Dnajb1都被认为是氧化应激的标志物。作者研究了Ahrr-/-IEL以寻找ROS暴露的迹象,运用小提琴图描绘了Ahrr-/-IEL比WT IEL对ROS表达更高水平的反应基因。因此scRNA-seq表明IEL需要Ahrr来防止过量的ROS(图 3)。
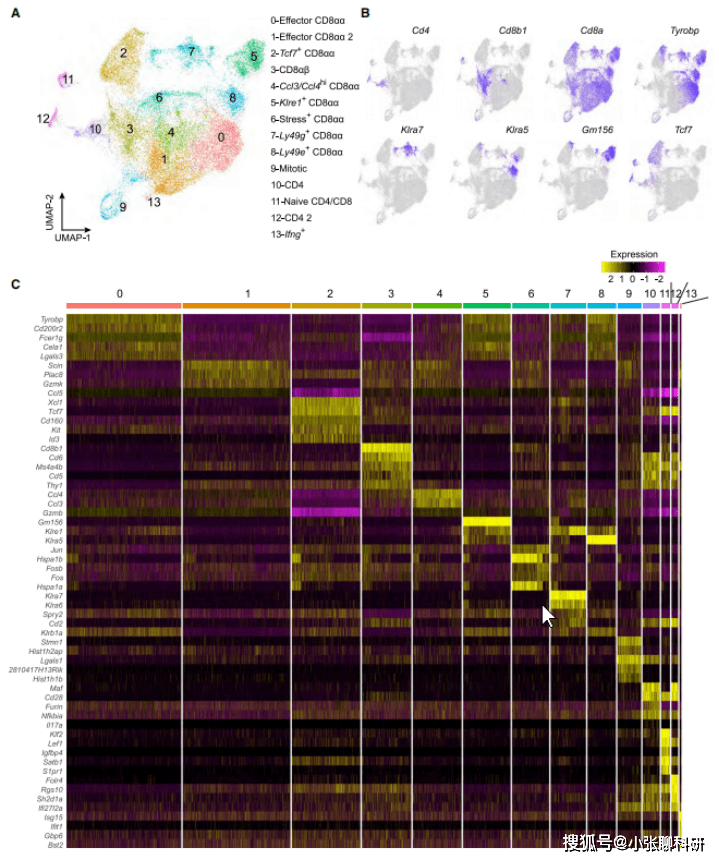
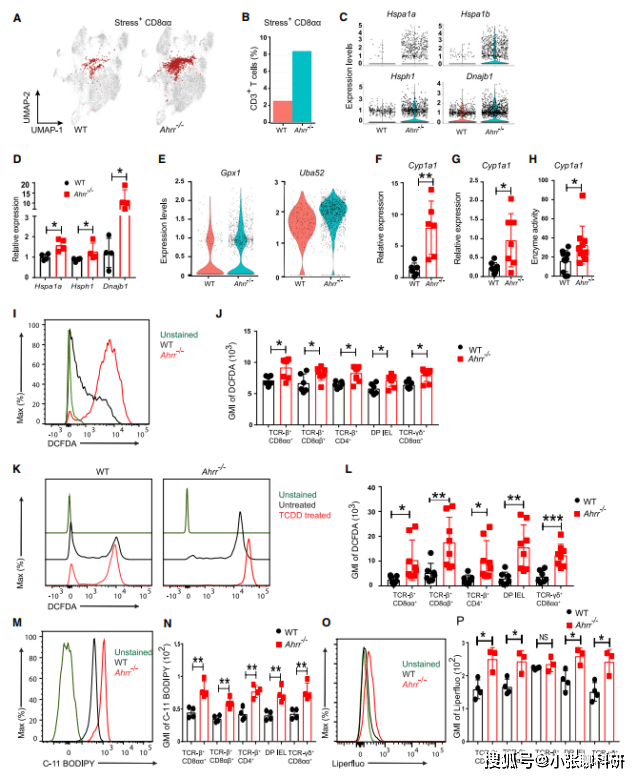
前期研究表明,CYP家族的酶在代谢其底物时产生ROS。此外,CYPs将花生四烯酸代谢为脂质代谢物,增加NADPH氧化酶活性,进一步导致ROS产生。那么Ahrr-/-IEL中的氧化应激反应是否由于Ahr-CYP1A1 轴失调,导致CYP1A1酶活性增加以及ROS产生?作者通过 qPCR 分析出Cyp1a1 mRNA在Ahrr-/-小鼠回肠组织中表达更多,TCDD(Ahr 配体和CYP1A1的底物)刺激后Ahrr-/-小鼠IEL中的CYP1A1酶活性更高、ROS产生更多。ROS 已被证明会引起脂质过氧化和铁死亡,作者用C-11 BODIPY(一种脂质过氧化标记)染色、Liperflou(铁死亡标志物)流式细胞术和显微镜观察证实了Ahrr-/-IEL 脂质过氧化相较于WT IEL显著增加。
为了直接验证CYP1A1在诱导铁死亡中的作用,作者对编码CYP1A1的逆转录病毒转导的T细胞系进行C-11 BODIPY染色,检测出CYP1A1转导的细胞脂质过氧化增加,rhapontigenin抑制CYP1A1后Ahrr-/-IEL中TCDD诱导的脂质过氧化降低(图 4)。
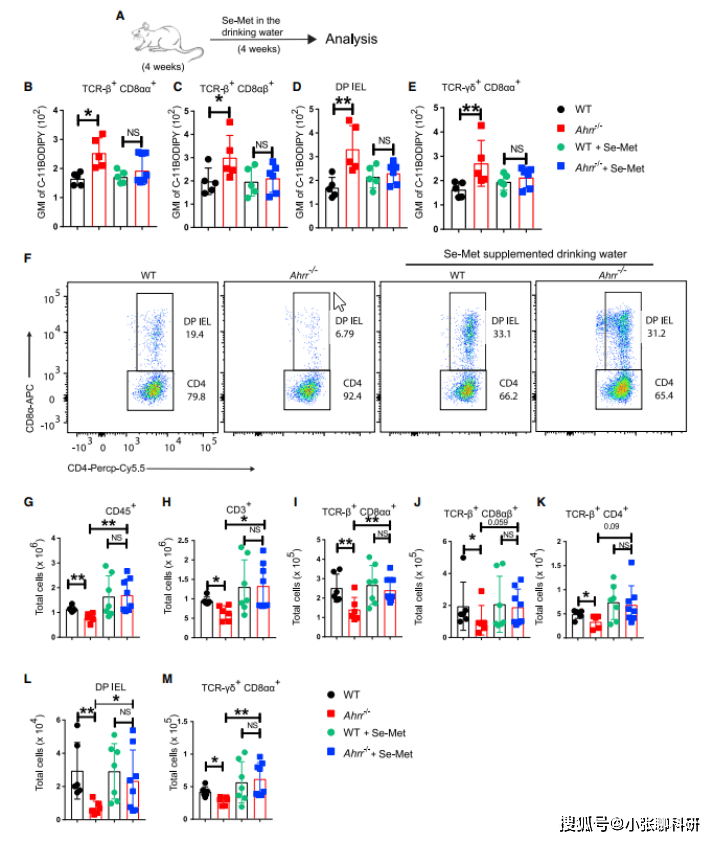
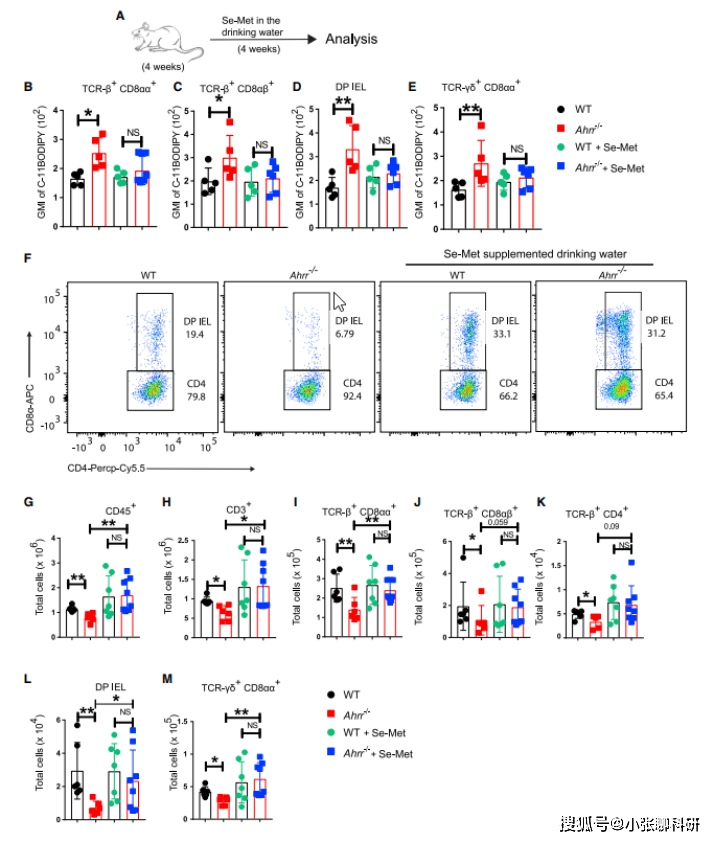
由于硒和硒蛋白、Vit-E能够抑制铁死亡和脂质过氧化,因此作者测试了膳食补充硒、Vit-E补充剂是否可以挽救Ahrr-/-小鼠的IEL损失,发现硒饮用水处理组以及Vit-E补充剂处理组Ahrr-/-IEL的过氧化作用均减少到与WT IEL相当水平,Ahrr-/-IEL数量则增加到与WT IEL数量相似(图 5)。进一步证实了Ahrr-/-小鼠的IEL 损失是由ROS生成增加以及诱导铁死亡引起的。
我们了解到Ahrr缺失是怎样影响IEL数量的,为了进一步确定Ahrr缺失对IEL降低所带来的功能影响,作者检测了Ahrr-/-和WT小鼠稳态回肠组织中各种炎症标志物(如 Tnfa、Ifng 和 IL-6)的表达,结果并无显著性差异,表明Ahrr缺失不会自发引起组织炎症。接着,作者通过建立艰难梭菌感染模型,发现Ahrr-/-小鼠比WT小鼠更易感染艰难梭菌,感染后Ahrr-/-小鼠肠组织中炎症标志物和抗菌肽基因的mRNA表达明显减少,并且Ahrr缺失对T细胞具有内在影响。先前实验表明,Ahrr-/-小鼠更容易受到DSS诱导的结肠炎,那么是否由于IEL的缺失造成的?作者比较了DSS诱导的结肠炎和DSS治疗前3天用WT IELs重建的Ahrr-/-小鼠结肠炎严重程度,结果表明IEL的过继转移保护Ahrr-/-小鼠免受结肠炎的侵害。
如前所述,Ahrr缺失对T细胞具有内在影响,为了探讨Ahrr对人类肠道T细胞的影响,作者通过检查免疫细胞图谱确定了Ahrr主要由组织驻留记忆gd T细胞和肠道巨噬细胞表达。另外,作者想知道Ahrr表达在IBD中受到的影响,对CD患者的手术标本进行IELs频率和功能表征分析,发现在炎症组织中Ahrr的表达低于非炎症组织,这一结果与相同样本中报告的gd T细胞频率降低一致。因此,Ahrr表达与肠道炎症呈负相关,提示Ahrr可能与肠道炎症的发病机制有关。
文章发现调节Ahr信号以保护IEL免受铁死亡以及保持肠道免疫反应的重要性。Ahr诱导其自身的负调节因子Ahrr,这种负反馈循环对IEL的维持至关重要。Ahrr缺失一方面增强Ahr介导的CYP1A1酶活性,诱导ROS过量产生,从而引发IEL脂质过氧化和铁死亡,另一方面也会增加肠道病理的易感性。作者认为膳食补充抗氧化元素硒或维生素 E有望挽救IEL缺失。
鉴于Ahrr在平衡Ahr信号转导中的作用,作者推测Ahrr表达降低可能通过促进人类IEL中ROS的产生和铁死亡来促进IBD的发病。未来的研究将确定IBD中Ahrr的表达降低是主要事件还是继发于与IBD发病机制相关的Ahr信号失调。
ayx中国官方网站


 京公网安备 11010802028692号
京公网安备 11010802028692号
 北京客服1
北京客服1